Vaskulärer endothelialer Wachstumsfaktor A (VEGFA): Ein Eckpfeiler der Angiogenese und darüber hinaus
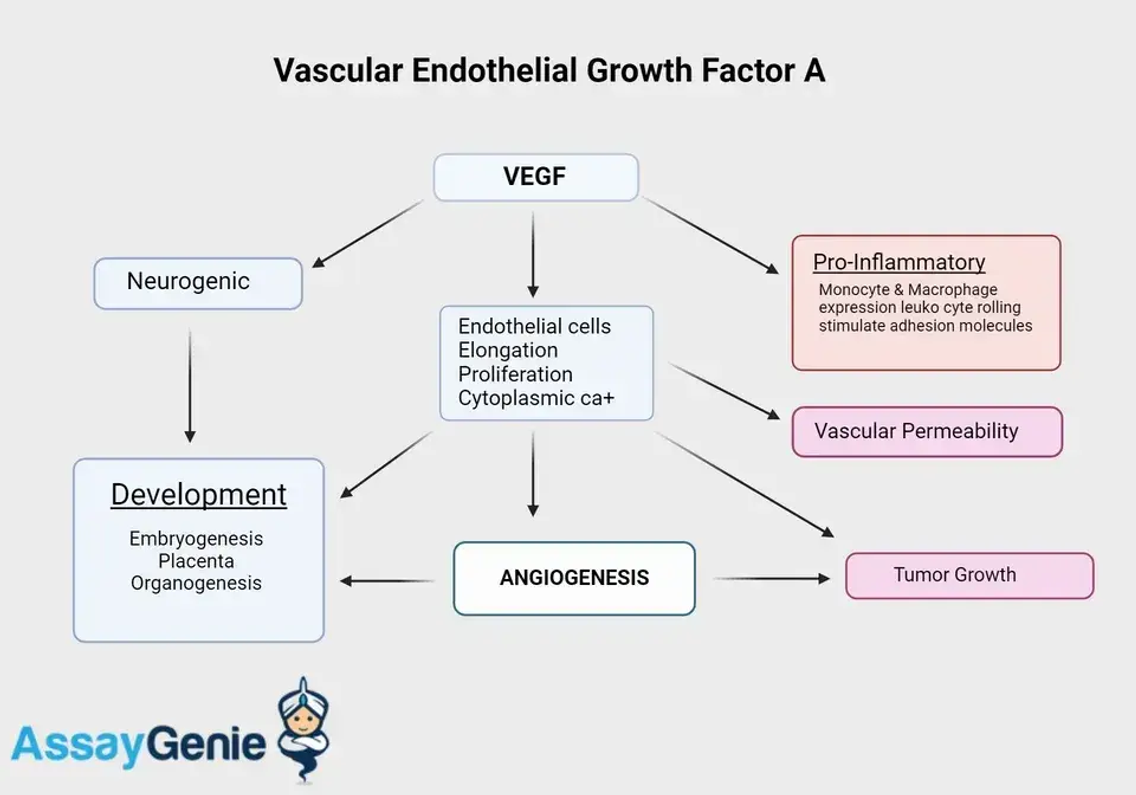
Der vaskuläre endotheliale Wachstumsfaktor A (VEGFA) ist ein zentrales Signalprotein, das sowohl an der Vaskulogenese als auch an der Angiogenese beteiligt ist. Dabei handelt es sich um Prozesse, die für die Bildung von Blutgefäßen während der Embryonalentwicklung und das Wachstum neuer Blutgefäße aus bereits vorhandenen wichtig sind. Als Mitglied der VEGF-Familie spielt VEGFA eine entscheidende Rolle bei der Regulierung der Endothelzellfunktion und beeinflusst die Gefäßpermeabilität und die Endothelzellproliferation.
Die Molekularbiologie von VEGFA
VEGFA zeichnet sich durch sein Gen auf Chromosom 6p21.1 aus, das für ein Heparin-bindendes Protein kodiert, das das Wachstum, die Migration und das Überleben von Endothelzellen fördert. Das VEGFA-Protein unterliegt komplexen posttranslationalen Modifikationen, die seine Bioverfügbarkeit und Aktivität beeinflussen. Durch alternatives Spleißen des VEGFA-Gens entstehen mehrere Isoformen, wobei VEGFA165 die am häufigsten vorkommende und biologisch aktive Form ist. Diese Isoformen unterscheiden sich in ihrer Fähigkeit, an VEGF-Rezeptoren (VEGFRs) und Co-Rezeptoren zu binden, was zu unterschiedlichen biologischen Wirkungen führt.
Tabelle: Eigenschaften der wichtigsten VEGFA-Isoformen
Isoform | Aminosäuren | Eigenschaften | Bindung an VEGFRs | Hauptfunktionen |
VEGFA121 | 121 | Frei diffundierbar, bindet kein Heparin | VEGFR-1, VEGFR-2 | Angiogenese, minimale Rolle bei der Gefäßpermeabilität |
VEGFA165 | 165 | Am häufigsten, bindet Heparin | VEGFR-1, VEGFR-2, Neuropiline | Angiogenese, Gefäßpermeabilität, Endothelzellmigration |
VEGFA189 | 189 | Bindet Heparin stark und wird in der extrazellulären Matrix gebunden | VEGFR-1, VEGFR-2, Neuropiline | Die Angiogenese, die an der Bildung von Fenstern beteiligt ist, hat die biologische Aktivität abgesondert |
VEGFA206 | 206 | Bindet Heparin stark und wird in der extrazellulären Matrix gebunden | VEGFR-1, VEGFR-2, Neuropiline | Ähnlich wie VEGFA189, begrenzte Verfügbarkeit aufgrund der starken Matrixbindung |
Physiologische Rollen von VEGFA
VEGFA ist maßgeblich an physiologischen Prozessen beteiligt, die über die Angiogenese hinausgehen, einschließlich der Wundheilung und des weiblichen Fortpflanzungszyklus. Es verbessert die Gefäßpermeabilität und ermöglicht so einen effizienten Austausch von Nährstoffen und Abfallprodukten zwischen Blut und Gewebe. In der Embryonalentwicklung steuert VEGFA die Bildung des Herz-Kreislauf-Systems. Seine Expression wird durch hypoxische Bedingungen streng reguliert, wobei der Hypoxie-induzierbare Faktor 1 (HIF-1) ein wichtiger vorgeschalteter Regulator ist und sicherstellt, dass die VEGFA-Spiegel auf den Sauerstoffbedarf des Gewebes reagieren.
VEGFA bei Krankheiten
Eine Fehlregulation der VEGFA-Expression ist mit verschiedenen Krankheiten verbunden, insbesondere mit solchen, die eine abnormale Angiogenese und Gefäßpermeabilität beinhalten. Bei Krebs fördert VEGFA das Tumorwachstum und die Metastasierung, indem es die Versorgung mit Sauerstoff und Nährstoffen durch die Bildung neuer Blutgefäße verbessert. Es spielt auch eine wichtige Rolle bei der altersbedingten Makuladegeneration (AMD), bei der eine übermäßige VEGFA-Aktivität zu einer pathologischen Angiogenese in der Netzhaut und damit zu Sehverlust führt.
Therapeutische Anwendungen und Herausforderungen
Die Entdeckung der Rolle von VEGFA bei Krankheiten hat zur Entwicklung von Anti-VEGFA-Therapien geführt, vor allem gegen Krebs und AMD. Diese Behandlungen, einschließlich monoklonaler Antikörper und löslicher Rezeptoren, zielen darauf ab, die VEGFA-Signalübertragung zu hemmen. Das therapeutische Targeting von VEGFA bringt jedoch Herausforderungen mit sich, wie z. B. Resistenzen gegen eine antiangiogene Therapie bei Krebspatienten und mögliche Nebenwirkungen im Zusammenhang mit einer beeinträchtigten physiologischen Angiogenese und Wundheilung.
Neue Forschung und zukünftige Richtungen
Aktuelle Forschung konzentriert sich auf die Aufklärung der komplexen Regulation von VEGFA und seinen Rezeptoren, die Identifizierung neuer therapeutischer Ziele und die Entwicklung wirksamerer und sichererer Behandlungen. Besonders vielversprechend sind Studien, die die Rolle von VEGFA in der regenerativen Medizin untersuchen, beispielsweise im Tissue Engineering und bei der Behandlung ischämischer Erkrankungen.
Ethische und gesellschaftliche Implikationen
Die Manipulation des VEGFA-Spiegels wirft ethische und gesellschaftliche Fragen auf, insbesondere im Zusammenhang mit der Steigerung der sportlichen Leistung oder der unbefugten Anwendung antiangiogener Therapien. Die möglichen langfristigen Auswirkungen einer Veränderung eines grundlegenden Prozesses wie der Angiogenese erfordern eine sorgfältige Abwägung und Regulierung.
Abschluss
VEGFA ist ein entscheidendes Molekül in der Gefäßbiologie und spielt eine weitreichende Rolle bei Gesundheit und Krankheit. Während Therapien, die auf VEGFA abzielen, sich als vielversprechend erwiesen haben, sind fortlaufende Forschungsarbeiten unerlässlich, um seine Funktionen vollständig zu verstehen und wirksamere und sicherere Therapiestrategien zu entwickeln. Die Zukunft der VEGFA-Forschung birgt großes Potenzial zur Verbesserung der menschlichen Gesundheit bei einem Spektrum von Krankheiten.
Verweise
1. Ferrara, N., et al. (2003). „Entdeckung und Entwicklung von Bevacizumab, einem Anti-VEGF-Antikörper zur Behandlung von Krebs.“ Nature Reviews Drug Discovery, 2(5), 391-400.
2. Shibuya, M. (2011). „Vaskulärer endothelialer Wachstumsfaktor (VEGF) und sein Rezeptorsignal (VEGFR) bei der Angiogenese: Ein entscheidendes Ziel für anti- und proangiogene Therapien.“ Genes & Cancer, 2(12), 1097-1105.
3. Carmeliet, P. & Jain, R.K. (2011). „Molekulare Mechanismen und klinische Anwendungen der Angiogenese.“ Natur, 473(7347), 298-307.
4. Kim, K.J., et al. (1993). „Die Hemmung der durch den vaskulären endothelialen Wachstumsfaktor induzierten Angiogenese unterdrückt das Tumorwachstum in vivo.“ Natur, 362(6423), 841-844.
5. Leung, D.W., et al. (1989). „Der vaskuläre endotheliale Wachstumsfaktor ist ein sezerniertes angiogenes Mitogen.“ Science, 246(4935), 1306-1309.
6. Ferrara, N. (2004). „Vaskulärer endothelialer Wachstumsfaktor: Grundlagenforschung und klinischer Fortschritt.“ Endocrine Reviews, 25(4), 581-611.
7. Holmes, D.I.R. & Zachary, I. (2005). „Die Familie der vaskulären endothelialen Wachstumsfaktoren (VEGF): Angiogene Faktoren für Gesundheit und Krankheit.“ Genombiologie, 6(2), 209.
8. Gerber, H.P., et al. (1999). „VEGF reguliert das Überleben hämatopoetischer Stammzellen durch einen internen autokrinen Schleifenmechanismus.“ Natur, 417(6892), 954-958.
16th Jul 2024
Recent Posts
-
Neuroimmunologie: Das Immunsystem des ZNS
…30th Sep 2024 -
Interleukin-8-Signalisierung
IL-8-ÜbersichtInterleukin-8 (IL-8), auch bekannt als CXCL8, wurde vor über 30 Jahren a …25th Sep 2024 -
Waardenburg-Syndrom und Klein-Waardenburg-Syndrom
Waardenburg-Syndrom: Eine seltene genetische Störung, die Pigmentierung, Hörvermögen u …25th Sep 2024