Thrombozytenadhäsionsproteine und Liganden: Schlüsselakteure bei Hämostase und Thrombose
Die Blutplättchenadhäsion ist ein entscheidender Prozess bei der Aufrechterhaltung der Blutstillung, der Reaktion des Körpers auf Blutungen. Dieser komplizierte Prozess beinhaltet eine Reihe von Wechselwirkungen zwischen Blutplättchen, den zellulären Bestandteilen des Blutes, und dem Gefäßendothel, der inneren Auskleidung der Blutgefäße. Im Zentrum dieses Prozesses stehen spezifische Proteine und Liganden, die die ersten Schritte der Blutplättchenadhäsion, -aktivierung und -aggregation vermitteln und letztendlich zur Bildung eines Blutplättchenpfropfens führen, der die Blutstillung unterstützt. Dieser Artikel befasst sich mit den lebenswichtigen Rollen von Thrombozytenadhäsionsproteinen und ihren Liganden und beleuchtet ihre Bedeutung sowohl im physiologischen als auch im pathologischen Kontext.
Thrombozytenadhäsion verstehen:
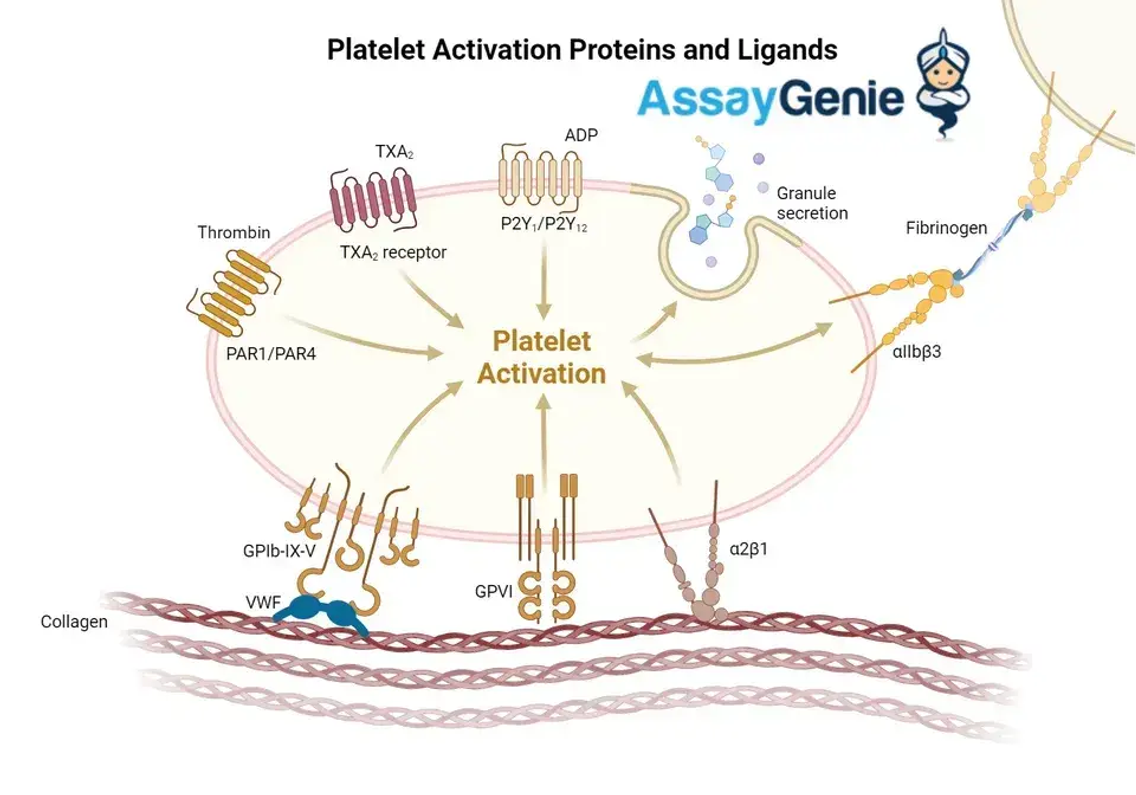
Die Blut plättchen adhäsion ist der grundlegende Schritt bei der Bildung eines hämostatischen Pfropfens, ein Prozess, der bei einer Gefäßverletzung ausgelöst wird. Dieser Prozess wird durch ein komplexes Netzwerk aus Adhäsionsproteinen und ihren Liganden vermittelt und erleichtert die Verankerung von Blutplättchen an der Verletzungsstelle. Unter diesen Proteinen spielen der Glykoprotein (GP) Ib-IX-V-Komplex, GP VI und Integrine eine zentrale Rolle.

Abbildung: Thrombozytenaktivierungsmechanismus
Glykoprotein-Ib-IX-V-Komplex: Das Tor zur Thrombozytenaktivierung:
Der GPIb-IX-V-Komplex ist ein Thrombozytenoberflächenrezeptorkomplex, der für die Thrombozytenadhäsion an der subendothelialen Matrix unter Bedingungen hoher Scherspannung von entscheidender Bedeutung ist. Der Von-Willebrand-Faktor (vWF), ein multimeres Protein, das im Plasma und im Subendothel vorkommt, dient als Hauptligand für den GPIb-IX-V-Komplex. Die Wechselwirkung zwischen vWF und GPIb-IX-V ist für das anfängliche Einfangen von Blutplättchen an der Stelle der Gefäßverletzung von entscheidender Bedeutung, erleichtert deren Rollen auf dem Endothel und trägt zur Rekrutierung zusätzlicher Blutplättchen für den wachsenden Thrombus bei.
GP VI: Der Kollagenrezeptor:
GP VI ist ein Schlüsselrezeptor für Kollagen, einem weiteren Hauptbestandteil der subendothelialen Matrix, die bei Gefäßverletzungen freigelegt wird. Die Bindung von GP VI an Kollagen löst eine Signalkaskade aus, die zur Aktivierung der Blutplättchen, zur Formänderung und zur Freisetzung von Granulatinhalten führt, wodurch die Blutplättchenaggregation und die Stabilisierung des Blutplättchenpfropfens weiter gefördert werden.
FuIntegrins: Überbrückung der Thrombozytenadhäsion und -aggregation:
Integrine, insbesondere αIIbβ3 (auch bekannt als GPIIb/IIIa), sind integraler Bestandteil des Prozesses der Blutplättchenaggregation. Nach der Aktivierung der Blutplättchen unterliegen Integrine einer Konformationsänderung, die ihre Affinität zu Fibrinogen erhöht, einem Plasmaprotein, das als Brücke zwischen Blutplättchen dient und deren Aggregation erleichtert. Die Bindung von Fibrinogen an das αIIbβ3-Integrin ist ein entscheidender Schritt bei der Bildung des Blutplättchenpfropfens und unterstreicht die Bedeutung von Integrinen für die Blutstillung.
Pathologische Auswirkungen der Blutplättchenadhäsion:
Während die Adhäsion von Blutplättchen für die Hämostase von entscheidender Bedeutung ist, kann eine Fehlregulation dieses Prozesses zu pathologischen Zuständen wie Thrombose, der Bildung eines Blutgerinnsels in einem Blutgefäß, führen, was den Blutfluss behindern und zu ischämischen Ereignissen führen kann. Überaktive Blutplättchenadhäsion und -aggregation können zur Entwicklung einer arteriellen Thrombose beitragen, einer Hauptursache für Myokardinfarkt und Schlaganfall. Umgekehrt können Mängel an Thrombozytenadhäsionsproteinen oder deren Liganden, wie das Bernard-Soulier-Syndrom (verbunden mit GPIb-IX-V-Komplex-Mangel) oder die von-Willebrand-Krankheit (gekennzeichnet durch defekten vWF), zu Blutungsstörungen aufgrund einer beeinträchtigten Thrombozytenfunktion führen.
Abschluss
Thrombozytenadhäsionsproteine und ihre Liganden spielen eine zentrale Rolle im Prozess der Blutstillung und vermitteln die ersten Schritte der Thrombozytenadhäsion, -aktivierung und -aggregation. Das Verständnis der molekularen Mechanismen, die diesen Wechselwirkungen zugrunde liegen, liefert Einblicke in das empfindliche Gleichgewicht, das für eine ordnungsgemäße hämostatische Kontrolle erforderlich ist, und zeigt potenzielle therapeutische Ziele für die Behandlung von Thrombose- und Blutungsstörungen auf. Fortschritte in unserem Verständnis der Thrombozytenbiologie werden weiterhin die Entwicklung neuartiger Therapiestrategien zur Modulation der Thrombozytenfunktion bei Krankheiten beeinflussen.
Verweise
1. Ruggeri, Z.M. (2002). Blutplättchen bei Atherothrombose. Naturmedizin, 8(11), 1227-1234.
2. Andrews, R.K., Berndt, M.C. (2004). Thrombozytenphysiologie und Thrombose. Thrombosis Research, 114(5-6), 447-453.
3. Clemetson, K. J., Clemetson, J. M. (2001). Thrombozytenkollagenrezeptoren. Thrombose und Hämostase, 86(1), 189-197.
4. Savage, B., Saldivar, E., Ruggeri, Z.M. (1996). Initiierung der Thrombozytenadhäsion durch Arretierung auf Fibrinogen oder Translokation auf den von Willebrand-Faktor. Zelle, 84(2), 289-297.
5. Jackson, S.P. (2007). Die wachsende Komplexität der Blutplättchenaggregation. Blut, 109(12), 5087-5095.
6. Nieswandt, B., Watson, S.P. (2003). Thrombozyten-Kollagen-Interaktion: Ist GPVI der zentrale Rezeptor? Blut, 102(2), 449-461.
7. Shattil, S. J., Newman, P. J. (2004). Integrine: Dynamische Gerüste für Adhäsion und Signalübertragung in Blutplättchen. Blut, 104(6), 1606-1615.
8. Berndt, M.C., Andrews, R.K. (2013). Thrombozytenphysiologie und Thrombose. Thrombosis Research, 112(6), 424-430.
26th Jul 2024
Recent Posts
-
Neuroimmunologie: Das Immunsystem des ZNS
…30th Sep 2024 -
Interleukin-8-Signalisierung
IL-8-ÜbersichtInterleukin-8 (IL-8), auch bekannt als CXCL8, wurde vor über 30 Jahren a …25th Sep 2024 -
Waardenburg-Syndrom und Klein-Waardenburg-Syndrom
Waardenburg-Syndrom: Eine seltene genetische Störung, die Pigmentierung, Hörvermögen u …25th Sep 2024