STING-Aktivatoren als Krebstherapeutika
Der STING-Signalweg (Stimulator of Interferon Genes) spielt eine zentrale Rolle bei der Reaktion des angeborenen Immunsystems auf Krebszellen und DNA-Viren. Die Nutzung dieses Signalwegs durch STING-Aktivatoren stellt einen vielversprechenden Weg für Krebs therapeutika dar. Dieser Artikel befasst sich mit dem Wirkmechanismus von STING-Aktivatoren, ihrem therapeutischen Potenzial, den Herausforderungen bei ihrer Entwicklung und den neuesten Fortschritten auf diesem Gebiet.
Den STING-Signalweg verstehen
Die biologische Rolle von STING
Der STING-Signalweg ist ein wesentlicher Bestandteil der angeborenen Immunantwort und weist zytosolische DNA nach, um die Produktion von Typ-I-Interferonen und anderen Zytokinen auszulösen. Diese Reaktion ist entscheidend für die Fähigkeit des Immunsystems, Infektionen zu bekämpfen und bösartige Zellen zu erkennen.
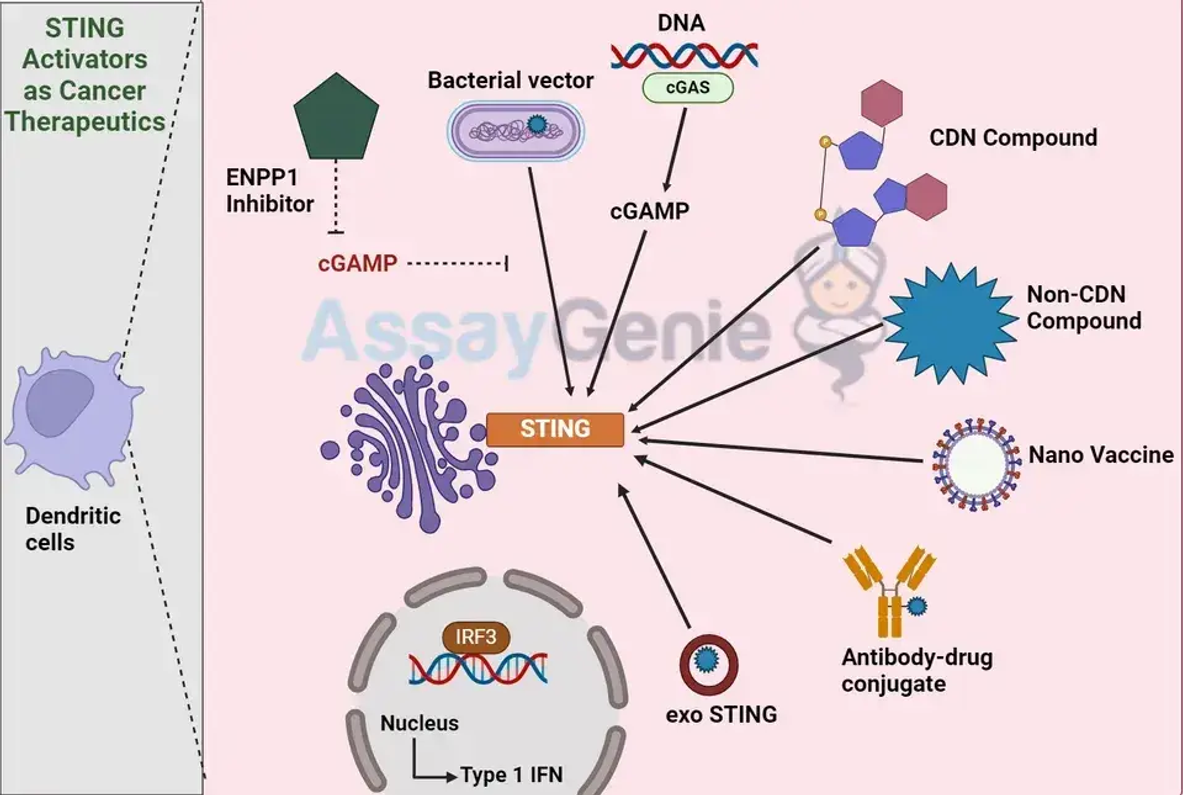
Die STING-Aktivierung erfolgt durch die Detektion von zyklischen Dinukleotiden (CDNs), die entweder endogen produziert oder extern eingeführt werden. Nach der Bindung an diese CDNs erfährt STING eine Konformationsänderung, die eine Signalkaskade in Gang setzt, die in der Aktivierung von Transkriptionsfaktoren wie IRF3 und NF-κB gipfelt und zur Produktion von Typ-I-Interferonen und proinflammatorischen Zytokinen führt.
STING-Aktivatoren in der Krebstherapie
Begründung für die Verwendung von STING-Aktivatoren
Der Grund für den Einsatz von STING-Aktivatoren in der Krebstherapie liegt in ihrer Fähigkeit, eine robuste Immunantwort gegen Tumore zu induzieren. Durch die Aktivierung des STING-Signalwegs können diese Wirkstoffe die Sichtbarkeit von Krebszellen für das Immunsystem verbessern und ihre Ausscheidung fördern.
STING-Aktivatoren bergen ein erhebliches therapeutisches Potenzial, das sich in präklinischen Modellen in ihrer Fähigkeit zeigt, Tumore zu verkleinern. Herausforderungen wie die Sicherstellung eines selektiven Targetings von Tumorzellen, die Vermeidung systemischer Entzündungen und die Überwindung der immunsuppressiven Tumormikroumgebung bleiben jedoch bestehen.
Fortschritte bei der Entwicklung von STING-Aktivatoren
Neuartige STING-Aktivatoren und ihre Mechanismen
Jüngste Fortschritte auf diesem Gebiet haben zur Entwicklung neuartiger STING-Aktivatoren mit verbesserten pharmakokinetischen Eigenschaften und erhöhter Spezifität für den STING-Signalweg geführt. Dazu gehören Modifikationen am CDN-Rückgrat und die Entwicklung von nicht-nukleotiden STING-Agonisten.
Klinische Studien und Ergebnisse
Mehrere STING-Aktivatoren befinden sich derzeit in klinischen Studien, wobei die ersten Ergebnisse in Bezug auf Sicherheit und anfängliche Wirksamkeit vielversprechend sind. Diese Studien sind entscheidend für die Bestimmung der optimalen Dosierungsschemata, Verabreichungswege und Kombinationen mit anderen Krebstherapien.
Widerstände überwinden und Wirksamkeit steigern
Innovationen und Forschungsrichtungen, die darauf abzielen, aktuelle Herausforderungen zu bewältigen, wie z. B. Kombinationstherapien, die Entdeckung von Biomarkern und neuartige Checkpoint-Targets, werden diskutiert und beleuchten die Zukunft der Krebsbehandlung.
Tabelle: Wichtige STING-Aktivatoren in der Entwicklung
Name des Aktivators | Kunst | Wirkmechanismus | Phase der klinischen Studie |
Verbindung A | Synthetisches CDN | Ahmt endogene CDNs nach und aktiviert STING direkt | Phase I |
Verbindung B | Nicht-Nukleotid-Agonist | Bindet an STING und induziert eine Konformationsänderung | Phase II |
Verbindung C | Geändertes CDN | Verbesserte Stabilität und Spezifität für STING | Präklinische |
Abschluss
STING-Aktivatoren stellen eine neuartige Klasse von Krebstherapeutika dar, die das Potenzial haben, die Behandlung verschiedener Krebsarten zu revolutionieren. Während ihre Entwicklung und klinische Anwendung nach wie vor Herausforderungen zu bewältigen sind, verbessern laufende Forschungen und klinische Studien unser Verständnis und unsere Fähigkeit, den STING-Signalweg für die Krebstherapie nutzbar zu machen, rasant.
Verweise
- Barber, G.N. (2015). STING: Infektion, Entzündung und Krebs. Nature Reviews Immunologie, 15(12), 760-770.
- Corrales, L.,
et al. (2015). STING-Aktivierung für die Krebsimmuntherapie. Trends in der Immunologie, 36(11), 677-684. - Deng, L., et
al. (2014). Die STING-abhängige zytosolische DNA-Sensorik fördert die strahleninduzierte Typ-I-Interferon-abhängige Antitumorimmunität in immunogenen Tumoren. Immunität, 41(5), 843-852. - Miao L, Qi J, Zhao Q, Wu QN, Wei DL, Wei XL, Liu J, Chen J, Zeng ZL, Ju HQ, Luo HY, Xu
RH. Die Ausrichtung auf den STING-Signalweg in tumorassoziierten Makrophagen reguliert die angeborene Immunwahrnehmung von Magenkrebszellen. Theranostik. 1. Januar 2020; 10(2):498-515. DOI: 10.7150/THNO.37745. PMID:
31903134; PMCID: PMC6929973. - Ohkuri, T.,et al. (2014). STING trägt zur Antitumorimmunität in einem syngenen Mausmodell bei. Krebsimmunologie-Forschung, 2(5), 403-414.
- Ribas, A.,Wolchok, J.D. (2018). Krebsimmuntherapie mit Checkpoint-Blockade. Wissenschaft, 359(6382), 1350-1355.
- Wilson, E.B.,et al. (2013). Blockade des chronischen Typ-I-Interferon-Signalwegs zur Kontrolle einer persistierenden LCMV-Infektion. Wissenschaft,
340(6129), 202-207. - 8. Gan Y, Li X, Han S, Liang Q, Ma X, Rong P, Wang W, Li W. Der cGAS/STING-Signalweg: Ein neuartiges Ziel für die Krebstherapie. Front Immunol. 3. Januar 2022;12:795401. DOI: 10.3389/fimmu.2021.795401. PMID: 35046953; PMCID: PMC8761794.
Recent Posts
-
Neuroimmunologie: Das Immunsystem des ZNS
…30th Sep 2024 -
Interleukin-8-Signalisierung
IL-8-ÜbersichtInterleukin-8 (IL-8), auch bekannt als CXCL8, wurde vor über 30 Jahren a …25th Sep 2024 -
Waardenburg-Syndrom und Klein-Waardenburg-Syndrom
Waardenburg-Syndrom: Eine seltene genetische Störung, die Pigmentierung, Hörvermögen u …25th Sep 2024