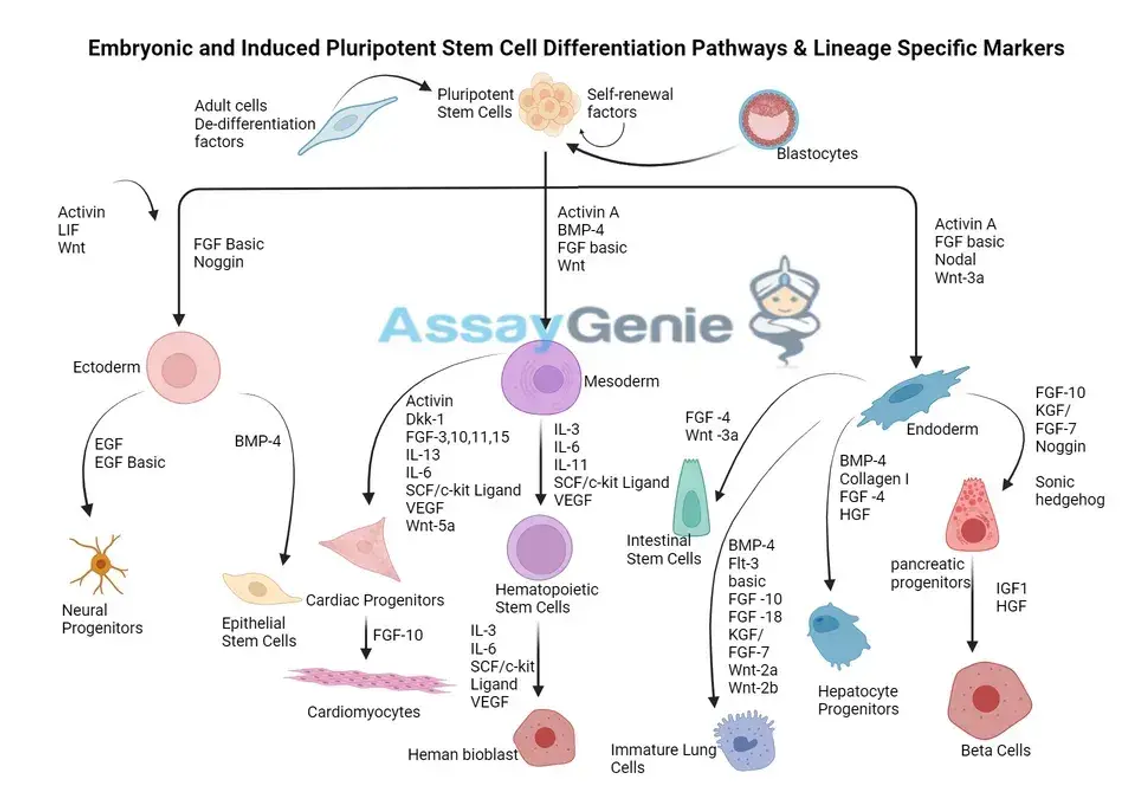
Embryonal induzierte Differenzierung pluripotenter Stammzellen: Wege und linienspezifische Marker
Embryonal induzierte pluripotente Stammzellen (iPSCs) bergen aufgrund ihrer Fähigkeit, sich in verschiedene Zelltypen zu differenzieren, ein enormes Potenzial im Bereich der regenerativen Medizin. Das Verständnis der Differenzierungswege und die Identifizierung linienspezifischer Marker sind für die Weiterentwicklung der Stammzell forschung und -therapie von entscheidender Bedeutung.
Überblick über die embryonale iPSC-Differenzierung:
Embryonale iPSCs zeichnen sich durch ihre Pluripotenz aus, die Fähigkeit, sich in jeden Zelltyp der drei primären Keimblätter zu differenzieren: Ektoderm, Mesoderm und Endoderm. Diese Pluripotenz wird durch spezifische Transkriptionsfaktoren wie Oct4, Sox2 und Nanog aufrechterhalten. Der Differenzierungsprozess beinhaltet ein komplexes Zusammenspiel dieser Faktoren und führt zur Spezialisierung in verschiedene Zelllinien.

Abbildung: Embryonal induzierte Differenzierungswege pluripotenter Stammzellen und linienspezifische Markierung
Ektoderm-Differenzierung:
Das Ektoderm ist die äußerste Schicht der drei Keimschichten und bildet den Ursprung des Nervensystems und der Haut. Zu den Schlüsselmarkern für die ektodermale Differenzierung gehören Sox1, PAX6 und Nestin. Diese Marker sind entscheidend für die Identifizierung der Entwicklung neuronaler Vorläuferzellen und Epidermiszellen.
- Sox1: Ein Marker für frühe neuronale Vorläufer.
- PAX6: Wichtig für die Neuralleisten- und Augenentwicklung.
- Nestin: Wird in neuralen Stammzellen exprimiert.
Mesoderm-Differenzierung:
Das Mesoderm, die mittlere Keimschicht, bildet Herz, Blut, Knochen und Muskeln. T (Brachyury) ist ein primärer Marker für die mesodermale Differenzierung, der die Entwicklung von mesenchymalen Stammzellen, Herzzellen und hämatopoetischen Linien anzeigt.
- T (Brachyury): Ein Transkriptionsfaktor, der für die Mesodermbildung essentiell ist.
- CD34: Ein Marker für hämatopoetische Vorläufer.
- MyoD: Spezifisch für die Muskelzelllinie.
Endoderm-Differenzierung:
Das Endoderm bildet innere Strukturen wie Lunge, Leber und Bauchspeicheldrüse. Sox17 ist ein entscheidender Marker für die endodermale Differenzierung und steuert die Entwicklung von Hepatozyten und Pankreaszellen.
Bedeutung und Anwendungen:
Das Verständnis dieser Differenzierungswege und Marker ist für stammzellbasierte Therapien von entscheidender Bedeutung. Es ermöglicht die präzise Entwicklung gewünschter Zelltypen zur Behandlung verschiedener Krankheiten wie Diabetes, Parkinson und Herzerkrankungen.
Abschluss:
Die embryonale iPSC-Differenzierung ist ein fein abgestimmter Prozess, der für den Fortschritt der regenerativen Medizin von entscheidender Bedeutung ist. Die Identifizierung linienspezifischer Marker wie Sox1, T und Sox17 bietet wesentliche Werkzeuge, um die Stammzelltherapie zu erfolgreichen klinischen Ergebnissen zu führen.
Referenzen
1. Takahashi, K. & Yamanaka, S. (2006). Induktion pluripotenter Stammzellen aus embryonalen und adulten Fibroblastenkulturen von Mäusen durch definierte Faktoren. Zelle, 126(4), 663-676.
2. Thomson, J. A., et al. (1998). Aus menschlichen Blastozysten gewonnene embryonale Stammzelllinien. Science, 282(5391), 1145-1147.
3. Boyer, L. A., et al. (2005). Zentraler Transkriptionsregulationsschaltkreis in menschlichen embryonalen Stammzellen. Zelle, 122(6), 947-956.
4. Chambers, I., et al. (2009). Nanog schützt die Pluripotenz und vermittelt die Keimbahnentwicklung. Natur, 450(7173), 1230-1234.
5. Murry, C. E. & Keller, G. (2008). Differenzierung embryonaler Stammzellen in klinisch relevante Populationen: Lehren aus der Embryonalentwicklung. Zelle, 132(4), 661-680.
6. Loh, Y. H., et al. (2006). Das Oct4- und Nanog-Transkriptionsnetzwerk reguliert die Pluripotenz in embryonalen Stammzellen von Mäusen. Nature Genetics, 38(4), 431-440.
7. Avilion, A. A., et al. (2003). Multipotente Zelllinien in der frühen Mausentwicklung hängen von der SOX2-Funktion ab. Genes & Development, 17(1), 126-140.
8. Tam, P. P. & Loebel, D. A. (2007). Genfunktion in der Embryogenese von Mäusen: Machen Sie sich bereit für die Gastrulation. Nature Reviews Genetics, 8(5), 368-381.
10th Aug 2024
Recent Posts
-
Neuroimmunologie: Das Immunsystem des ZNS
…30th Sep 2024 -
Interleukin-8-Signalisierung
IL-8-ÜbersichtInterleukin-8 (IL-8), auch bekannt als CXCL8, wurde vor über 30 Jahren a …25th Sep 2024 -
Waardenburg-Syndrom und Klein-Waardenburg-Syndrom
Waardenburg-Syndrom: Eine seltene genetische Störung, die Pigmentierung, Hörvermögen u …25th Sep 2024