Das Schicksal von Stammzellen mit Transkriptionsfaktoren steuern
Das Wesen von Stammzellen und ihre Bedeutung:
Transkriptionsfaktoren: Die Hauptregulatoren
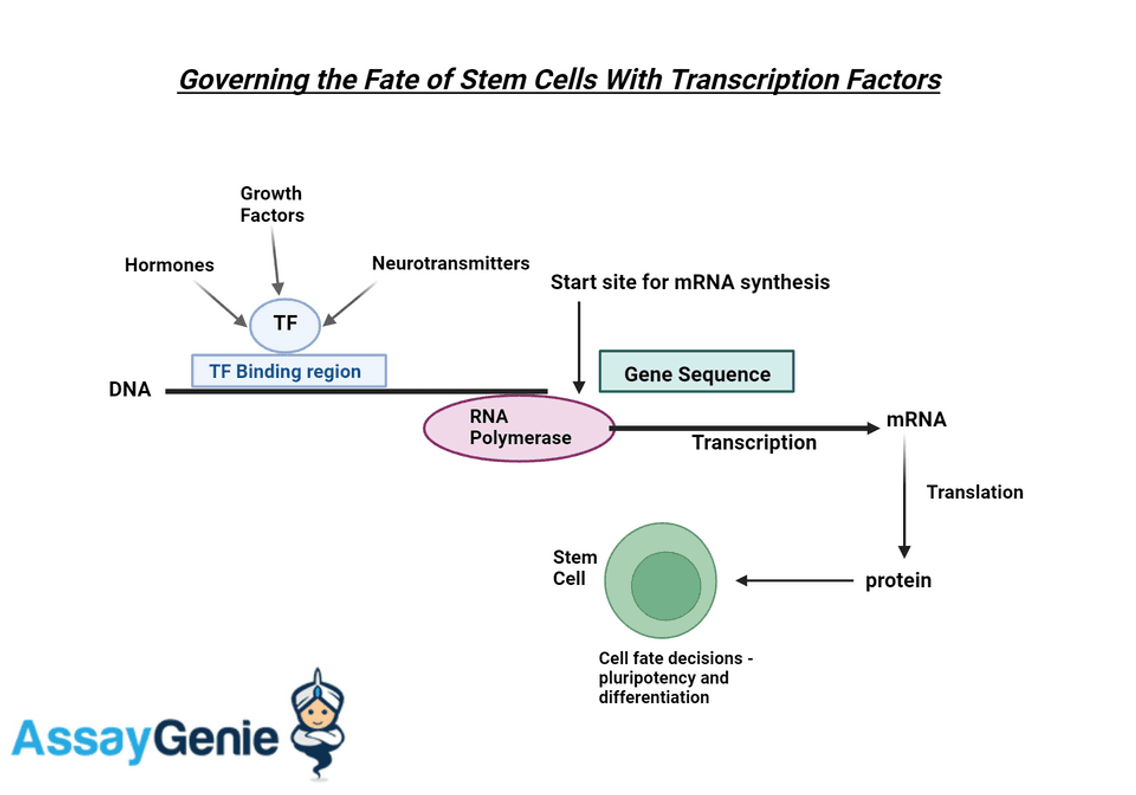
Transkriptionsfaktoren spielen eine entscheidende Rolle bei der Kontrolle des Schicksals von Stammzellen. Diese Proteine erfüllen ihre Funktion, indem sie an bestimmten Stellen an die DNA binden und so die Expression von Genen modulieren, die für die Aufrechterhaltung der Stammzellen oder die Auslösung von Differenzierungswegen wichtig sind. Ihre Fähigkeit, Gene ein- oder auszuschalten, macht sie unverzichtbar für die zelluläre Orchestrierung, die die Zellidentität bestimmt.
- Kerntranskriptionsfaktoren der Pluripotenz
In embryonalen Stammzellen ist ein Kernnetzwerk von Transkriptionsfaktoren, darunter OCT4, SOX2 und NANOG, entscheidend für die Aufrechterhaltung der Pluripotenz und der Selbsterneuerungsfähigkeiten. Insbesondere OCT4 gilt als Hauptregulator der Pluripotenz. Seine genauen Ausdrucksebenen sind entscheidend; Zu wenig oder zu viel kann zur Differenzierung in bestimmte Abstammungslinien bzw. zum Verlust der Pluripotenz führen.
- Transkriptionsfaktoren und Abstammungsspezifikation
Während sich Stammzellen auf den Weg zur Differenzierung machen, werden linienspezifische Transkriptionsfaktoren von zentraler Bedeutung. Beispielsweise wird der Übergang von ESCs in neurale Vorläuferzellen durch die Hochregulierung neuralspezifischer TFs wie PAX6 und SOX1 gesteuert, was die ersten Schritte in Richtung des Schicksals neuronaler oder glialer Zellen markiert.
Mechanismen der Wirkung des Transkriptionsfaktors:
Der Mechanismus, durch den Transkriptionsfaktoren das Schicksal von Stammzellen regulieren, beinhaltet eine Kombination aus direkter DNA-Bindung und Interaktion mit anderen zellulären Mechanismen wie epigenetischen Modifikatoren und nichtkodierenden RNAs. Dieses Interaktionsnetzwerk steuert nicht nur die Expression von Zielgenen, sondern auch den Chromatinzustand und beeinflusst dadurch die Zugänglichkeit und Expressionsprofile von Genen.
- Epigenetische Regulations- und Transkriptionsfaktoren
Transkriptionsfaktoren spielen auch eine entscheidende Rolle bei der epigenetischen Regulation, zu der Modifikationen wie DNA-Methylierung und Histonmodifikation gehören. Diese Modifikationen können die Chromatinstruktur verändern und dadurch die Zugänglichkeit von Transkriptionsfaktoren zu ihren Ziel-DNA-Sequenzen beeinträchtigen. Beispielsweise kann die Interaktion zwischen OCT4 und epigenetischen Regulatoren einen Chromatinzustand aufrechterhalten, der der Pluripotenz förderlich ist.
- Das dynamische Zusammenspiel mit nichtkodierenden RNAs
Nichtkodierende RNAs (ncRNAs), einschließlich microRNAs (miRNAs) und lange nichtkodierende RNAs (lncRNAs), stellen eine weitere Regulationsebene dar, an der Transkriptionsfaktoren beteiligt sind. Diese ncRNAs können die Expression und Aktivität von Transkriptionsfaktoren modulieren und so eine Ebene der posttranskriptionellen Regulierung hinzufügen, die die Entscheidungen über das Schicksal von Stammzellen weiter verfeinert.
Herausforderungen und Chancen in der Transkriptionsfaktorforschung:
Trotz der erheblichen Fortschritte beim Verständnis der Rolle von Transkriptionsfaktoren in der Stammzellbiologie bleiben Herausforderungen bestehen. Die Redundanz und Pleiotropie der Transkriptionsfaktoren sowie die Komplexität ihrer regulatorischen Netzwerke stellen erhebliche Hindernisse dar. Fortschritte bei Technologien wie CRISPR-Cas9 zur Genbearbeitung und Einzelzell-RNA-Sequenzierung bieten jedoch beispiellose Einblicke in die dynamischen Regulierungslandschaften, die das Schicksal von Stammzellen bestimmen.
Therapeutisches Potenzial der Transkriptionsfaktormodulation
Die Fähigkeit, das Schicksal von Stammzellen durch Modulation der Transkriptionsfaktoraktivität zu kontrollieren, birgt ein enormes therapeutisches Potenzial, insbesondere in der regenerativen Medizin und im Tissue Engineering. Strategien zur Umprogrammierung somatischer Zellen in induzierte pluripotente Stammzellen (iPSCs) durch die Einführung spezifischer Transkriptionsfaktoren haben das Gebiet bereits revolutioniert. Darüber hinaus bietet die direkte Umprogrammierung eines Zelltyps in einen anderen unter Umgehung eines pluripotenten Zustands vielversprechende Möglichkeiten zur Regeneration geschädigten Gewebes oder zur Behandlung degenerativer Erkrankungen.
Zukünftige Richtungen
Mit Blick auf die Zukunft wird die Erforschung von Transkriptionsfaktor-Netzwerken weiterhin Aufschluss über die komplexen Regelkreise geben, die das Verhalten von Stammzellen bestimmen. Das Verständnis dieser Netzwerke wirft nicht nur Licht auf grundlegende biologische Prozesse, sondern ebnet auch den Weg für innovative Therapiestrategien. Die fortlaufende Integration der Computerbiologie mit der experimentellen Forschung verspricht, die Komplexität der durch Transkriptionsfaktoren vermittelten Regulierung zu entschlüsseln und neue Werkzeuge und Ziele für die Manipulation des Schicksals von Stammzellen zu bieten.
Abschluss
Zusammenfassend lässt sich sagen, dass Transkriptionsfaktoren für die Regulierung des Schicksals von Stammzellen von zentraler Bedeutung sind und das Gleichgewicht zwischen Pluripotenz und Differenzierung durch ein komplexes Netzwerk genetischer und epigenetischer Mechanismen steuern. Mit fortschreitender Forschung auf diesem Gebiet wächst das Potenzial, diese Mechanismen für therapeutische Anwendungen zu nutzen, und verspricht neue Horizonte in der regenerativen Medizin und darüber hinaus.
Verweise
1. Takahashi, K. & Yamanaka, S. (2006). Induktion pluripotenter Stammzellen aus embryonalen und adulten Fibroblastenkulturen von Mäusen durch definierte Faktoren. Zelle, 126(4), 663-676.
2. Boyer, L. A., Lee, T. I., Cole, M. F., Johnstone, S. E., Levine, S. S., Zucker, J. P., ... & Young, R. A. (2005). Zentraler Transkriptionsregulationsschaltkreis in menschlichen embryonalen Stammzellen. Zelle, 122(6), 947-956.
3. Young, RA (2011). Kontrolle des embryonalen Stammzellzustands. Zelle, 144(6), 940-954.
4. Ng, H. H. & Surani, M. A. (2011). Die Transkriptions- und Signalnetzwerke der Pluripotenz. Nature Cell Biology, 13(5), 490-496.
5. Graf, T. & Enver, T. (2009). Zellen dazu zwingen, ihre Abstammungslinie zu ändern. Natur, 462(7273), 587-594.
6. Orkin, S. H. & Hochedlinger, K. (2011). Chromatin-Verbindungen zu Pluripotenz und zellulärer Neuprogrammierung. Zelle, 145(6), 835-850.
7. Wapinski, O. L. & Chang, H. Y. (2011). Lange nichtkodierende RNAs und menschliche Krankheiten. Trends in Cell Biology, 21(6), 354-361. Zhou, Q.,
8. Melton, D. A. (2008). Extreme Umgestaltung: Umwandlung einer Zelle in eine andere. Zellstammzelle, 3(4), 382-388.
20th Jul 2024
Recent Posts
-
Neuroimmunologie: Das Immunsystem des ZNS
…30th Sep 2024 -
Interleukin-8-Signalisierung
IL-8-ÜbersichtInterleukin-8 (IL-8), auch bekannt als CXCL8, wurde vor über 30 Jahren a …25th Sep 2024 -
Waardenburg-Syndrom und Klein-Waardenburg-Syndrom
Waardenburg-Syndrom: Eine seltene genetische Störung, die Pigmentierung, Hörvermögen u …25th Sep 2024